Plan de l'article
Mémoires physiologiques
Le nez a une triple fonction : respirant, immunisé, aux aérocontaminants et aux odeurs. Le nez traite environ 10 000 litres d’air par jour, qui est filtré, humidifié et réchauffé. Les sinus apparaissent comme des cavités physiologiquement muets, dont l’homéostasie est déterminée par les caractéristiques de la membrane muqueuse et de l’ostie. L’anatomie des sinus ne se souvient pas ici, mais peut être facilement récupérée dans les livres de référence.
La muqueuse sinusale se compose d’un épithélium des voies respiratoires pseudo-couches, qui est caractérisé par une fréquence relative des cellules muqueuses qui compensent la rareté des glandes séro-muqueuses du chorion. La muqueuse sinusale est capable d’absorber l’oxygène et de jeter du dioxyde de carbone. Les mesures en boucle fermée donnent des valeurs moyennes de 2,2 % de CO2 et 17,5 % d’O2.
A voir aussi : Guérir d'une maladie infectieuse : méthodes efficaces et conseils pratiques
La température intrasinique est constante et hydrométrie près de 100%. La pression intrasinique est en équilibre avec la pression atmosphérique. Le reniflement crée une surpression allant jusqu’à 200 mm H2O dans les sinus, tandis que le reniflement peut provoquer un approfondissement de 180 mm H2O. Le renouvellement constant de l’air dans les sinus (entre 9 et 30 minutes) par Ostia compense l’échange transmuqueux. Toutes ces fonctions essentielles peuvent être perturbées par diverses pathologies qui seront discutées au cours de cet article.
Symptomatologie clinique et orientation diagnostique
Deux catégories de patients peuvent être imaginées en consultation ORL : les premiers patients, asymptomatiques, consulter après la détection radiologique d’une ou plusieurs sinusopaktias. L’enquête doit s’efforcer d’obtenir une symptomatologie aussi minimale qui puisse guider le diagnostic. En ce qui concerne la deuxième catégorie, ce sont les patients présentant un ou plusieurs symptômes qui doivent essayer de se référer aux images radiologiques.
A lire aussi : Boissons à éviter pour diabétiques : les trois pires choix à bannir pour votre santé
Lors de l’ examen, un ou plusieurs des symptômes suivants doivent être notés : obstruction nasale, rhinorrhée antérieure et/ou postérieure, dysosmie, agologies faciales, toux (luxations sèches ou postérieures), éternuements, prurit nasal et pharyngé, épistaxis et otite présive. Selon le diagnostic mentionné, d’autres symptômes sont liés.
La combinaison de ces symptômes en combinaison avec un examen clinique endoscopique rigoureux permet au médecin d’établir un diagnostic et d’offrir un traitement. Tous les diagnostics qui seront discutés font l’objet de nombreuses publications et livres. Le but de cet article est simplement de mettre en évidence l’approche ORL de la dysfonction sinueuse nasale chronique (DNSC).
La consultation en cas de troubles de l’odeur ou de dysosmie doit avoir le caractère quantitatif (hyposmie, anosmie) et qualitatif (cacosmie, parosmie et phantosmie) pour établir un diagnostic topographique et étiologique. La cacosémie (perception d’une ou plusieurs mauvaises odeurs) doit avoir une origine naso-sinusale (sinusite d’origine dentaire, aspergillome endosinique) ou une origine digestive (reflux gastro-œsophagien).
Les étiologies de l’hypo- ou de l’anosmie sont fréquentes.
Quatre étiologies méritent d’être mentionnées dans cet article :
- La polypose nasosinusienne (NSP) est la cause la plus fréquente de dysosmie due à une altération du transfert à l’aéroport. Le diagnostic est clinique lors de l’examen endoscopique.
- Les dysosmies après la rhinite allergique chronique ou non allergique sont connues, mais leur incidence est difficile à quantifier.
- La dysomie après la rhinite infectieuse virale est la principale cause d’hyposmie au monde. On croit qu’il est associé à la destruction des est liée aux neurones olfactifs et touche principalement les femmes (65 %) âgées de 50 à 60 ans. À ce jour, il n’y a pas de traitement, et en l’absence de récupération jusqu’à un an, la dysosmie est considérée comme finale.
- Une cause centrale de dysosmie, en dehors de celles liées à l’âge : la maladie d’Alzheimer, dans laquelle l’implication olfactive est précoce. La difficulté aujourd’hui est de provoquer la maladie d’Alzheimer avant l’anosmie progressive chez un patient de moins de 65 ans.
Raison fréquente de consultation, rhinorrhée postérieure (sensation de « décharge dans la gorge postérieure ») est isolée ou associée à des symptômes pharyngés (paresthésie pharyngée) et des symptômes laryngés (hémome, dysphonie, toux…).
Si cette rhinorrhée est antérieure, son caractère séreux, mucopurulent ou purulent conduit le diagnostic. Un cas particulier est la rhinorrhée séreuse du sujet âgé (« gouttes sur le nez « ) a été augmentée en raison des changements de température. C’est un dysfonctionnement nasal neurovégétatif et le bromure d’ipratropium réduit cette rhinorrhée.
Si la rhinorrhée séreuse s’accompagne d’éternuements, de prurit nasal ou pharyngé, de larmoiement, le diagnostic choisi est celui de la rhinite allergique chronique. Le caractère permanent ou intermittent dépend de la durée des symptômes. Plus de 4 jours par semaine ou plus de 4 semaines consécutives par an définissent la rhinite allergique permanente. Une évaluation allergologique par des tests cutanés permet de déterminer les allergènes responsables. La thérapie antihistaminique, combinée ou non avec la corticothérapie nasale, la désensibilisation sublinguale ou sous-cutanée sont les principaux éléments de l’arsenal thérapeutique du praticien.
L’ obstruction nasale, seule ou en association, est le plus souvent signalée par les patients. Cette gêne fonctionnelle peut être uni- soit bilatérale, complète ou partielle, dans la vie quotidienne, pendant l’effort physique ou peut être aggravée par des escarres. Dans le cas du ronflement, le praticien doit examiner l’interrogatoire (échelle Epworth – 1991 Dr. John’s Murray) pour les éléments en faveur du syndrome d’apnée du sommeil hypopnée (OSA), puis effectuer un enregistrement du sommeil (polygraphie de ventilation nocturne) ou dans la structure de l’hôpital (polysomnographie) à la maison. Dans le cas de l’OSA, diverses solutions sont discutées avec le patient (ventilation assistée, orthodontie avancée, parfois chirurgie…), mais n’oubliez jamais de prendre un excès de poids.
Les algies faciales ou les maux de tête sans signes rhinologiques associés peuvent-ils être d’origine rhinosinus si le patient présente un scan avec des opacités sinusales au médecin ? L’analyse sémiologique de la douleur doit être précise, afin de ne pas s’égarer dans le diagnostic. Reconnaissant la grandes tables semi-ologiques d’algies faciales va au-delà du champ d’application de l’article. Le praticien doit détecter et différencier une migraine commune sans aura, une migraine avec aura, une névralgie faciale essentielle ou non, une algie vasculaire du visage, une hémicranija paroxystique chronique, un syndrome SUNCT (Nevralgiforme unilatérale courte durée avec injection conjonctivale et déchirure)… La différenciation de ces étiologies permet de fournir au patient un traitement opportun et adéquat. L’arsenal thérapeutique à notre disposition est diversifié : anti-inflammatoires non stéroïdiens (indométhacine, kétoprofène), ripans familiaux, vérapamil, lithium, méthysergides, carbamazépine… Après tout, le praticien sera en mesure de provoquer une origine dentaire, un dysfonctionnement de l’articulation temporo-mandibulaire.
Dans ces circonstances, l’opinion d’un collègue dentiste-chirurgiens et pour la Le diagnostic et la gestion de cette galerie faciale sont essentiels.
La dernière raison fréquente de consultation, épistaxis conduit à une approche diagnostique différente. Le plus souvent, ces épistaxis sont associés à une tache vasculaire ectasique et une simple cautérisation, chimique (nitrate d’argent, acide chromique) ou saignement électrique. L’examen endoscopique est systématique et ne devrait que confirmer le diagnostic des taches vasculaires. Bien sûr, n’oubliez pas de chercher une augmentation de l’hypertension artérielle. La détermination de la prothrombine et une mesure du rapport international normalisé (INR) complèteront les études chez les patients prenant des anticoagulants oraux.
Endoscopie de la cavité nasale
L’ étude de la cavité nasale est le prélude à la gestion de toute pathologie rhinosinusienne. Pendant longtemps, le manque rudimentaire de moyens disponibles, la connaissance de l’anatomie et de la physiopathologie a été noté enrichi par l’utilisation de nouvelles techniques d’exploration : examen optique et imagerie, mais principalement rhinomanométrie, rhinométrie acoustique, étude de la fonction mucociliaire…
Un moyen essentiel d’investigation pour toute ORL en consultation, l’endoscopie nasale, après une étude précise et une rhinoscopie avant le spéculum, permet dans la plupart des cas de distinguer un problème architectural d’un problème fonctionnel. Dans les pathologies fonctionnelles, cet examen permet le type de déficience inflammatoire (œdème, pus ou croûtes) et la topographie (localisée ou diffuse).
L’ endoscopie nasale peut être réalisée en utilisant une fibre de verre flexible et/ou avec une optique rigide, et plus récemment, l’endoscope vidéo permet de créer une image numérique. Cet examen est le plus souvent effectué sous anesthésie locale, qui est associée à une vasoconstriction (brins trempés ou 5% de xylocaïne vaporisé avec de la naphazoline) pour améliorer le confort du patient et faciliter le mouvement de l’optique.
Le nasofibroscope est constitué de fibres optiques flexibles d’un diamètre de 2,1 à 3,7 mm, sans canal opérateur et muni d’une béquille à 90°. L’utilisation du fibroscope est bimmanual, ce qui rend impossible de faire un geste qui lui est associé.
L’ endoscopie optique rigide nécessite une vision directe ou 30°, 2,7 mm pour les enfants et 4 mm chez les adultes. L’utilisation de l’optique rigide présente deux avantages : premièrement, la qualité d’image est optimale et n’a pas d’effet de distorsion ou de moiré. Ensuite, l’examen sous une optique rigide donne une main et permet ainsi, si nécessaire, l’aspiration, l’échantillonnage pour l’étude bactériologique, cytologique…
L’ endoscopie de la cavité nasale permet de détecter l’apparition de la muqueuse nasale, son inflammatoire ou non inflammatoire, la présence de œdème localisé ou diffus pour évaluer la présence de croûtes devant le septum et les cônes inférieurs. L’apparence (séreuse, muqueuse, purulente ou sanglante) et la fréquence des sécrétions sont évaluées en fonction de la localisation topographique. Cet examen devrait se concentrer sur l’évaluation rigoureuse des structures anatomiques et des régions de chaque cavité nasale : cloison, cônes inférieurs et moyens et chair, voûte choanale, recessus sphénoéthmoïdal, méat supérieur.
La viande est parfois difficile à explorer en raison d’un éperon vomérien, mais si possible, le cône moyen peut être doucement repoussé avec une spatule pour accéder à la partie supérieure du méat moyen, dans lequel passe l’écoulement ethmoïde antérieur et sinus frontal. Quantum aux cellules ethmoïdes postérieures et le moïde de coin, le haut du corps est leur lieu de drainage. Cette étude est complétée par des recherches sur le nasopharynx ou le cavum, ainsi que des canaux auditifs (anciennement trompes d’Eustache), dont le dysfonctionnement peut être abordé (très utile pour comprendre les accidents barotraumatiques du plongeur).
Après tout, en raison d’une meilleure connaissance de la physiopathologie des sinus et des progrès dans l’imagerie, en raison d’une meilleure connaissance de la photomie sinusale maxillaire à des fins diagnostiques, n’est presque plus réalisée.
Après l’enquête et l’examen endoscopique, le praticien a suffisamment d’éléments pour suggérer un diagnostic et différencier les pathologies de la muqueuse nasale diffuses ou localisées dans une zone topographique.
Imagerie
Lorsque le site d’imagerie (tomodensitométrie de la masse faciale, dentascan, tomodensitométrie des sinus) est important, le développement du diagnostic étiologique n’est pas indispensable, contrairement à l’examen endoscopique de la cavité nasale. Lors de l’exécution de l’imagerie doit être basée sur les données du Survey, examen endoscopique, mais aussi l’enregistrement récent des corticostéroïdes peuvent être interprétés en cas de divergence entre les images radiologiques et l’examen clinique. L’injection d’un agent de contraste iodé au cours d’une analyse n’est pas nécessaire, et si un processus tumoral est suspecté, l’IRM avec injection de gadolinium donne plus d’informations.
Les protocoles d’acquisition sont actuellement normalisés. De la capture hélicoïdale des sections axiales, les reconstructions informatiques permettent d’obtenir des images dans les sections coronaires et sagittales. Il convient que le prescripteur informe le radiologue si d’autres reconstructions (type panoramique dentaire sur l’Apex Dental and Sinus Land) sont souhaitables.
L’ imagerie par résonance magnétique (IRM) est complémentaire s’il y a un doute diagnostique pendant la CT (forme pseudotumorale de la sinusite chronique, polypose atypique unilatérale). Dans ordre préopératoire, il est impératif de clarifier les relations orbitales et méningées des processus expansifs développés en contact avec la base du crâne (méningocèle, mucocèle). Enfin, l’IRM permet diverses séquences qui ont pondéré T1, T2 et T1 après l’injection du produit de contraste pour distinguer la rétention des sinus et les zones de collecte, les muqueuses inflammatoires et les processus de tissu tumoral.
L’ exploration TDM permet une analyse architecturale précise des grottes naso-sinusales. Le praticien doit après des changements dans les relations anatomiques avec les structures orbitales (procidence du nerf optique), vasculaire (procidence des artères carotides internes) et neuroméningée adjacente (déhiscence des parois osseuses), ce qui peut augmenter le risque de chirurgie. L’étude des sections radiologiques dans les 3 niveaux, en corrélation avec une reconstruction 3D des différentes structures, permet au praticien de déterminer la pour comprendre les changements anatomiques de la meilleure façon possible.
La perméabilité de chaque cavité nasale est estimée. Ainsi, la courbure de la cloison est analysée, son caractère obstructif ou non, la présence de luxation chondrovomérer, le caractère hypertrophique des cornets inférieurs, la présence d’un cornet moyen pneumatique (Concha Bullosa), l’inversion de la courbure d’un grain moyen, la présence de Synechias… L’analyse des fentes olfactives et des lames blindées est effectuée systématiquement. Les déchirures osseuses spontanées visent la lame papyracée et le toit de l’ethmoïde. L’analyse aux rayons X évalue toute anomalie de la région ostioméatale qui interfère avec le drainage nasosinique, ce qui provoque une pathologie de confinement (pneumatique du processus unsiforme, procidence de la vessie ethmoïdale…). L’analyse et l’interprétation de l’opacité des sinus doivent être effectuées avec l’anamnèse du patient, la données d’entrevue et les résultats de l’examen endoscopique.
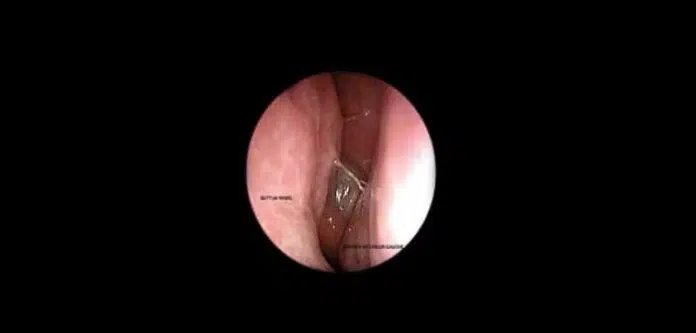
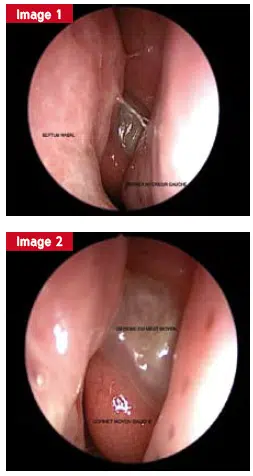
Parfois, le patient n’a aucun symptôme ou les symptômes décrits ne sont pas directement liés à la sinusopacité trouvée. Le plus souvent, il s’agit d’un kyste sous-muqueux ou muqueux (image arrondie, homogène, arêtes vives) localisé au fond du sinus maxillaire. Ce type d’image, contrairement au kyste mucocèle ou radiculus, ne crée aucun changement dans les parois osseuses. Le kyste muqueux (fig. 1 et 2) peut être associé à un épaississement de la muqueuse du sinus maxillaire (Fig. 3). L’examen endoscopique de l’ORL est alors important pour clarifier la perméabilité du complexe ostio-chair et pour éliminer la pathologie du confinement des sinus.
****** 0 Fig. 1 et 2 : Kyste du mucus du sinus maxillaire droit et remplissage du sinus maxillaire gauche. Patient avec Symptomatologie de la sinusite maxillaire gauche aiguë récurrente. Image de rétention sur IRM. Diagnostic peropératoire : muqueuse de la mâchoire gauche superinfectée. Fig. 3 : Épaississement du cadre de la muqueuse des sinus maxillaires
Cette vérification est d’autant plus importante qu’un projet implant dans la région du sinus maxillaire est considéré. La présence d’une hypertrophie radiologique des cônes inférieurs, qui s’accompagne de symptômes cliniques (obstruction nasale avec ou sans rhinorrhée antérieure et/ou prolongée), provoque une rhinite hypertrophique chronique. La corticothérapie locale est prescrite au patient et peut être complétée par cautérisation (chimique, laser ou radiofréquence). La prise en charge devient plus problématique si le patient signale des épisodes fréquents de « sinusite » ou s’il y a une obstruction radiologique du complexe ostioméatal. La corticothérapie locale dure plusieurs mois, accompagnée ou non corticothérapie générale permet parfois de détecter un canal auditif moyen en ce qui concerne l’inflammation isolée de la membrane muqueuse.
Cependant, l’examen endoscopique peut révéler une pathologie de confinement avec un œdème du méat moyen, une apparence polypoïde du cône moyen, ou même un polype par rapport au méat moyen. Si les traitements locaux sont inefficaces, le patient doit se voir offrir une viande endonasale moyenne pour reperméabiliser le conduit auditif moyen. Dans tous les cas, la communication entre les praticiens est essentielle pour optimiser et sécuriser le projet thérapeutique.
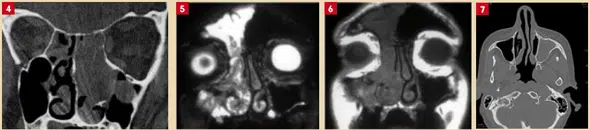
au moment de cette évaluation clinique et radiologique, seulement parfois un examen anatomopathologique permet d’établir un diagnostic étiologique. Cela s’applique au diagnostic d’un papillome inversé (Figues. 4, 5 et 6), un tumeur bénigne avec un développement lent et un potentiel malin. L’examen endoscopique trouve une lésion d’apparence papillomateuse, muriforme et souvent végétative. Le scanner confirme l’opacité unilatérale et recherche d’autres emplacements. Si la lyse osseuse est un bon élément diagnostique, elle n’est pas systématiquement présente. L’IRM est importante pour déterminer les extensions tumorales. Le traitement est chirurgical avec excision prolongée. Malheureusement, les répétitions sont fréquentes et nécessitent une surveillance stricte.
L’ opacité radiologique complète du sinus maxillaire et la présence d’une masse translucide du méat moyen en endoscopie devraient donner lieu à des soupçons de polypes killians ou d’un polype antrochoanal (Fig. 7). C’est une tumeur bénigne qui peut intéresser toute la cavité nasale, et dont le traitement est chirurgicalement endoscopique. Développé à partir de la muqueuse sinusale Mucocèle effectue un pseudokyste septique et provoque une lyse osseuse progressive avec prolifération ostéoblastique dans la périphérie. Le plus souvent, asymptomatique, mucocèle, primaire ou secondaire (chirurgie endosinusienne) est parfois révélé par des déformations associées à leur expansion, en particulier orbitale. Le scanner montre le plus souvent la sinusopacité ethmoïdale, mais peut intéresser tous les sinus du visage. Cette opacité est associée à l’ostéolyse avec reflux des structures de quartier. L’IRM estime le contenu de la muqueuse et son expansion dans le voisinage. Le traitement est chirurgical.
Fig. 4 : Symptomatologie de l’obstruction nasale unilatérale avec « gravité faciale » permanente. Remplissage de la fosse nasale par un gonflement muriforme, qui pendant l’endoscopie rappelle fortement le papillome inversé. Paralatéronasale élargie Opération. Diagnostic confirmé en anatomopathologie. Fig. 5 : papillome inversé, IRM hypersignal dans T1 Fig. 6 : papillome inversé, IRM isosignal T2 avec parenchyme cérébral Fig. 7 : polype de Killian ou polype antrochoanal. Le diagnostic a été provoqué avant l’obstruction nasale gauche avec rhinorrhée et litière postériotique pendant plusieurs années. Polype translucide par rapport au méat moyen. Otomie de viande avec excision complète de la lésion et examen anatomopathologique a confirmé le diagnostic.
De nombreux autres diagnostics sont discutés lors de l’examen des photographies radiologiques. Il ne s’agit pas de répéter toutes les étiologies énumérées dans cet article, mais de signaler les plus courantes.
Diagnostic étiologique
À la fin de la consultation avec l’examen endoscopique de la cavité nasale, un diagnostic est souvent offert. Examen clinique en combinaison avec le Cependant, dans la plupart des cas, la tomodensitométrie permet d’établir un diagnostic étiologique. D’autres études sont parfois nécessaires et seront discutées en fonction du diagnostic proposé. La pathologie nasosinique peut être classée en fonction de son évolution, aiguë ou chronique, assiégée, uni- ou bilatérale, son caractère, localisé ou diffus, ou selon des résultats anatomopathologiques bénins ou malins. Cependant, la classification de cette pathologie en fonction de l’apparence endoscopique (oedémateuse, purulente et incrustée), qui est en corrélation avec les images radiologiques, est plus appropriée pour la pratique quotidienne ORL.
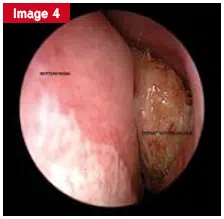
La pathologie œdémateuse (images 1 et 2), qui est le plus souvent diffuse et bilatérale, doit provoquer une polypose nasosinusique (SNP) (Figures 8 et 9) ou rhinosinusite oedémateuse chronique (RSCO). SNP – une maladie inflammatoire chronique de la muqueuse nasosinusienne est caractérisée par La présence de polypes dans la cavité nasale est caractérisée. Selon que les polypes passent le méat moyen ou non atteignent l’arrière de la corne inférieure ou non, 3 stades endoscopiques sont définis. L’enquête devra chercher des arguments en faveur de l’asthme. En cas de doute, des tests fonctionnels respiratoires (RFE) pour l’hyperréactivité bronchique doivent être effectués.
Fig. 1 : pathologie oedémateuse Fig. 2 : pathologie oedémateuse
L’ évaluation radiologique doit être effectuée en dehors d’une houle de surinfection et de préférence en dehors de la corticothérapie générale. Dans les premières formes, lorsque l’examen endoscopique est presque normal, la présence d’imcorps radiologiques bilatéraux d’intérêt pour les cellules ethmoïdes antérieures et postérieures indique le diagnostic d’ethmoïdite inflammatoire chronique. La présence d’hyperéosinophilie dans le Les sécrétions nasales (mais l’absence de normalisation de la méthode d’analyse cytologique) en l’absence d’allergie conduit au diagnostic de la rhinite non allergique avec éosinophilie (NARES), éthmoïdite éosinophile chronique.
Le traitement est basé sur une corticothérapie locale à long terme (au moins un an). En l’absence de traitement prolongé, des flambées évolutives se produisent et peuvent entraîner l’apparition de polypes. Diagnostiquer le RSCO est plus difficile que la polypose. L’inflammation avec œdème diffus doit être provoquée chez un patient présentant une obstruction nasale au moins 12 semaines par an de litière postérieure et lors de l’examen endoscopique. L’apparition de l’hyposmie devrait conduire à la recherche de polypose débutant nasosinique (Figure 3).
Pour l’enregistrement que la triade de la polypose nasosinique, l’asthme et l’intolérance combine l’aspirine et les AINS, y compris Les inhibiteurs de la COX 1, définissent la maladie de Wial.
Fig. 3 : Œdème du méat moyen
Contrairement à la pathologie oedémateuse, la pathologie purulente peut être uni- ou bilatérale. Le siège de rhinorrhée purulente suggère parfois la suspicion de l’origine de la suppuration : du pus devant la rainure incibuleuse sous la tête de la métacarine (sinus maxillaire, ethmoïde antérieur, sinus frontal), sphénoïd évidement (ethmoïde postérieur, sphénoïde). L’échantillonnage bactériologique dans l’une de ces deux régions n’est utile que pour les maladies chroniques. La technologie d’échantillonnage doit être prudente pour éviter la contamination et est réalisée avec un écouvillon qui doit être rapidement transporté au laboratoire.
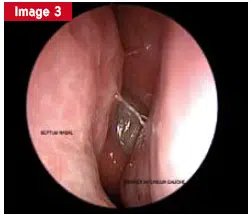
Avant la rhinorrhée postérieure (et parfois antérieure) unilatérale, mucopurulente avec obstruction nasale unilatérale, le praticien doit provoquer une étiologie dentaire, d’autant plus que le patient lui-même s’est plaint de Cacosmie. Le diagnostic est confirmé par la présence de pus du méat moyen. Tomodensitométrie objective Remplissage des sinus maxillaires partiel ou complet, qui est souvent associé au remplissage des cellules ethmoïdes antérieures, et parfois avec un remplissage partiel des sinus frontaux. L’ostéocondensation des parois sinusales provoque l’ancienneté de la pathologie infectieuse. La détection d’un granulome apical ou d’un kyste radulodental (Fig. 10) sur une prémolaire ou molaire confirme le diagnostic de sinusite d’origine dentaire. Le patient doit alors être dirigé vers un dentiste pour obtenir des soins dentaires appropriés. Il existe d’autres mécanismes de contamination du sinus maxillaire : migration d’un corps étranger (matériau de remplissage de canal, racine dentaire après l’extraction incidente, matériel implant anecdotique) (fig. 11 et 12), communication buccosinique (Fig. 13). Répond à tout mécanisme une attitude thérapeutique spécifique. La dernière pathologie cible est l’aspergillome sinusal (fig. 14 et 15). La localisation préférée est la mâchoire supérieure, et les soins dentaires se trouvent dans 2/3 des cas.
Figure 8 et 9 : polypose nasosinique Fig. 10 : kyste radiculodental. Symptomatologie de la sinusite maxillaire chronique gauche avec des flambées de surinfection pendant de nombreuses années. La turbinectomie gauche et inférieure de la viande, réalisée sans imagerie préopératoire, n’a pas alerté les épisodes infectieux. Et pour une bonne raison… Fig. 11 et 12 : Si le méat moyen est perméable, le dépassement ou la présence d’un implant dans le sinus maxillaire n’a pas nécessairement d’effets cliniques. D’autre part, s’il y a une pathologie d’arrêt du conduit auditif moyen, tout cambriolage de la muqueuse de l’endosinus avec la pénétration d’un corps étranger dans le sinus est responsable de l’infection Complications du sinus. Fig. 13 : Communication buccosinique
Pour 1/3, la physiopathologie est purement pure : pénétration des spores à travers l’ostium et développement de mycelhyphes. L’imagerie montre la calcification dans la moitié des cas, la sinusopacité hétérogène dans 40% des cas. L’examen mycologique est positif dans 95% des cas à l’examen direct. L’examen pathopathologique confirme la présence de filaments de mycélium dans 85% des cas.
Si la suppuration, malgré de multiples traitements antibiotiques, est bilatérale, chronique et récurrente, des études supplémentaires sur la mucoviscidose, la dyskinésie ciliaire primaire ou acquise et l’immunodéficience sont nécessaires. Une bronchorrhée avec toux dans ce contexte évoque la dilatation des bronches et doit être effectuée tomodensitométrie thoracique. La dernière forme clinique, moins souvent que les précédentes, est le nasosinique Pathologie de la croûte (Fig. 4). Selon que la maladie est isolée dans la cloison ou si elle présente un intérêt pour l’ensemble de la cavité nasale et/ou des sinus, divers diagnostics sont discutés. La biopsie est effectuée systématiquement dans les bourgeons localisés, infiltration, formes plus ou moins nécrotiques de carcinome épidermoïde, adénocarcinome (maladie professionnelle affectant les travailleurs du bois), mélanome ou lymphome non hodgkinien.
Pcd 4 : Pathologie croustillante
Dans les formes diffuses, plusieurs biopsies sont effectuées pour la sarcoïdose, la maladie de Wegener, le syndrome de Churg et Strauss. La pathologie croustillante est parfois iatrogène après une turbinectomie totale inférieure (technique maintenant prescrite), une radiothérapie externe ou une exposition professionnelle à certains agents toxiques.
trouve
L’ objectif principal de notre approche diagnostique est de comprendre les plaintes du patient, en les utilisant avec Pour corréler l’examen endoscopique de la cavité nasale et les résultats d’imagerie, puis avec l’aide d’études complémentaires pour essayer de comprendre les mécanismes ou les causes du patient afin d’offrir au patient un traitement étiologique et non symptomatique. En ce qui concerne notre approche thérapeutique, que ce soit médicalement et/ou chirurgicalement, un objectif essentiel est de soulager les affections fonctionnelles en essayant de rétablir les conditions nécessaires au fonctionnement physiologique du nez et des sinus.
Après tout, c’est cette rigueur qui doit permettre au praticien ORL, en collaboration avec ses collègues (dentiste, pneumologue, allergologue…) de proposer le (s) traitement (s) médical (s) approprié (s) et, si nécessaire, de proposer un geste chirurgical fonctionnel sur le nez (septoplastie liée à une opération de les cônes inférieurs, fonctionnement de la valve nasale…) et/ou sur les sinus (isocémie de viande moyenne, inférieure ; ethmoïdectomie antérieure ou totale…).
Bibliographie
1. P.Eoly, M.C.Nollevaux, B.Bertrand physiologie des sinus paranasaux. Otorhino- laryngol, Ed. Techniques, EMC (Paris, France), 20416 A10, 2005. 2. Jankowski R. Dysfonctionnement chronique de la nasosine. Rapport de la Société Française d’Otorhinolaryngologie et Chirurgie du Visage et du Cou. 2006. 3. Coquine C. Obstruction nasale. Rapport de la Société Française d’Otorhinolaryngologie et Chirurgie du Visage et du Cou. 1996. 4. Bonfils P., Jankowski R., Werner A. Les dysosmies d’origines naso-sinusienne. Revue de la Littérature. Ann Otolaryngol Chir Cervicofac 2001 ; 118:131 -142 5. Henkin R., Larson A., Powell R. Hypogueusia, dysguusie, hyposmie et dysosmie après infection grippale. Ann Otol 1985 ; 84:672 -82 6. Rhinite allergique et ses effets sur l’asthme (ARIA) 2008. European Journal of Allergy and Clinical Immunology, 2008 ; Supplément 86 : Volume 63 7. La Classification internationale des troubles des maux de tête 2e édition (ICHD-II) 2004 8. Shankar L., Evans K. Atlas de l’imagerie paranasale 2e édition Barnes & Noble 9. Les kystes de rétention de Bhattacharyya N. du sinus maxillaire reflètent les phénomènes sinus obstructifs Arch Otolaryngol Head Neck Surg, 2000:126:1369 -72 10. C. vilain, Fontanel JP., Peynegre R. La nasosinusienne polypose. Rapport de la Société Française d’Oto-rhino-laryngology et de Chirurgie de la Face et du Cou. 2000. 11. Bertrand B., Rombaux P., Eloy P., Reychler H. Sinusite d’origine dentaire. Acta Otorhinolaryngol Belg. 1997 ; 51 (4) :315-22 12. Yoskovitch A., Braverman I., MJ noir, papillome sur mesure sinonasale. Le Journal d’oto-rhino-laryngologie. 1998 ; 27 (3) :122-6 13. 14. Par Buchwald C., Larsen A. Chirurgie endoscopique des papillomes inversés sous guidage par image. Oto-rhino-laryngologie Chirurgie de la tête et du cou. 2005 ; 132 (4) : 602-7 Alobid I., Guilemany JM., Mullol J. Manifestations nasales des maladies systémiques. Curr Allergie Asthme Rep2004 ; 4 (3) :208-16